政策法規 || 2024年度藥品審評報告(附法規概覽3.17-3.21)
01
2024年度藥品審評報告
國家藥品監督管理局藥品審評中心發布2024年度藥品審評報告。

掃描圖中二維碼
查看詳細信息

02
國家藥監局綜合司公開征求《藥品試驗數據保護實施辦法(試行,征求意見稿)》《藥品試驗數據保護工作程序(征求意見稿)》意見
為促進藥品創新和仿制藥發展,完善藥品試驗數據保護制度,根據《藥品管理法實施條例》等相關規定,借鑒國際經驗,國家藥監局起草了《藥品試驗數據保護實施辦法(試行,征求意見稿)》(附件1)、《藥品試驗數據保護工作程序(征求意見稿)》(附件2),現向社會公開征求意見。

掃描圖中二維碼
查看詳細信息

03
關于公開征求ICH《E6(R3):藥物臨床試驗質量管理規范技術指導原則(GCP)》原則及附件1中文翻譯稿意見的通知
為推動新修訂的ICH指導原則在國內的平穩落地實施,我中心組織翻譯了《E6(R3):藥物臨床試驗質量管理規范技術指導原則(GCP)》原則及附件1。現對E6(R3)原則及附件1中文翻譯稿公開征求意見,為期1個月。

掃描圖中二維碼
查看詳細信息

01
截止2025年3月21日15:00本周發布252個待領取藥品批準證明文件,其中注射液59個,一致性評價品種13個。
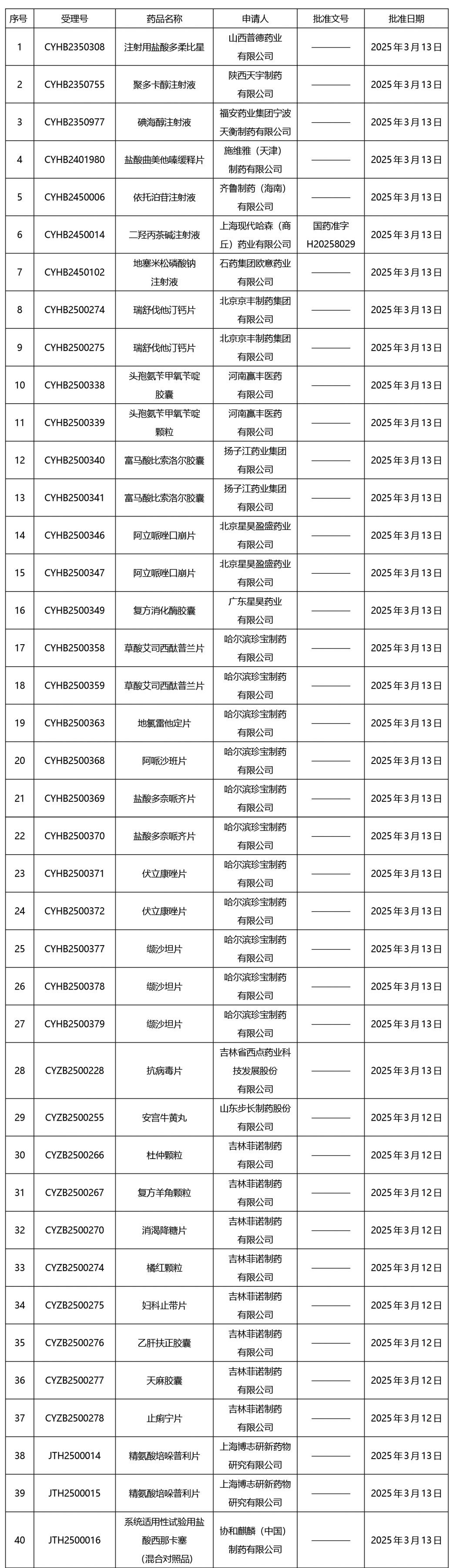
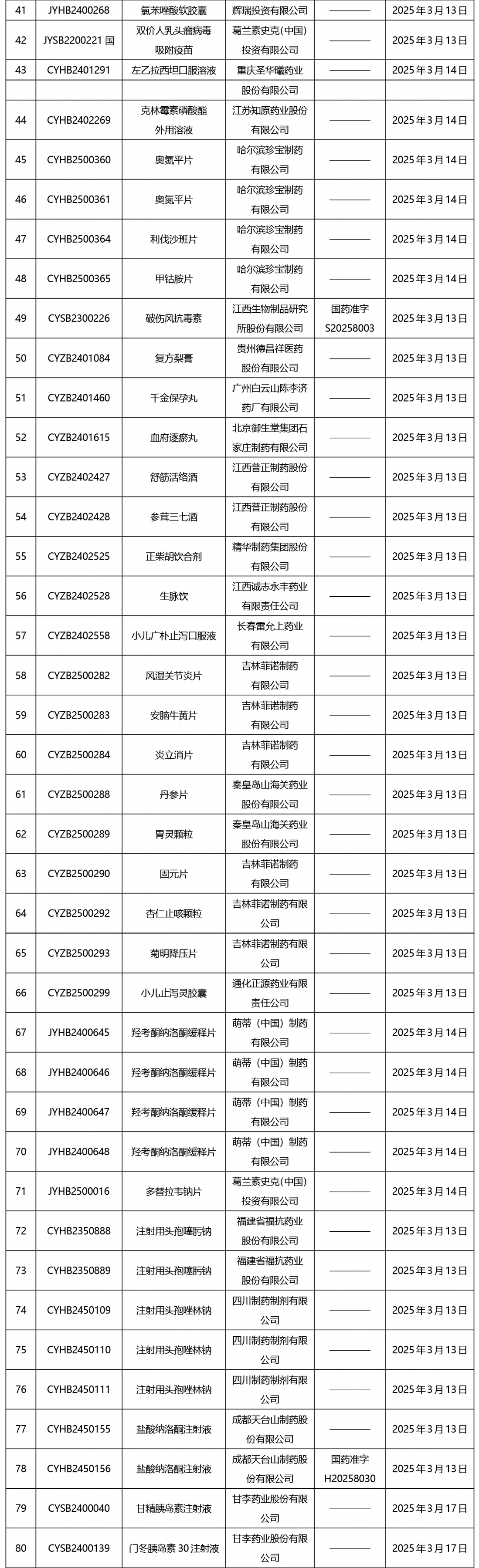
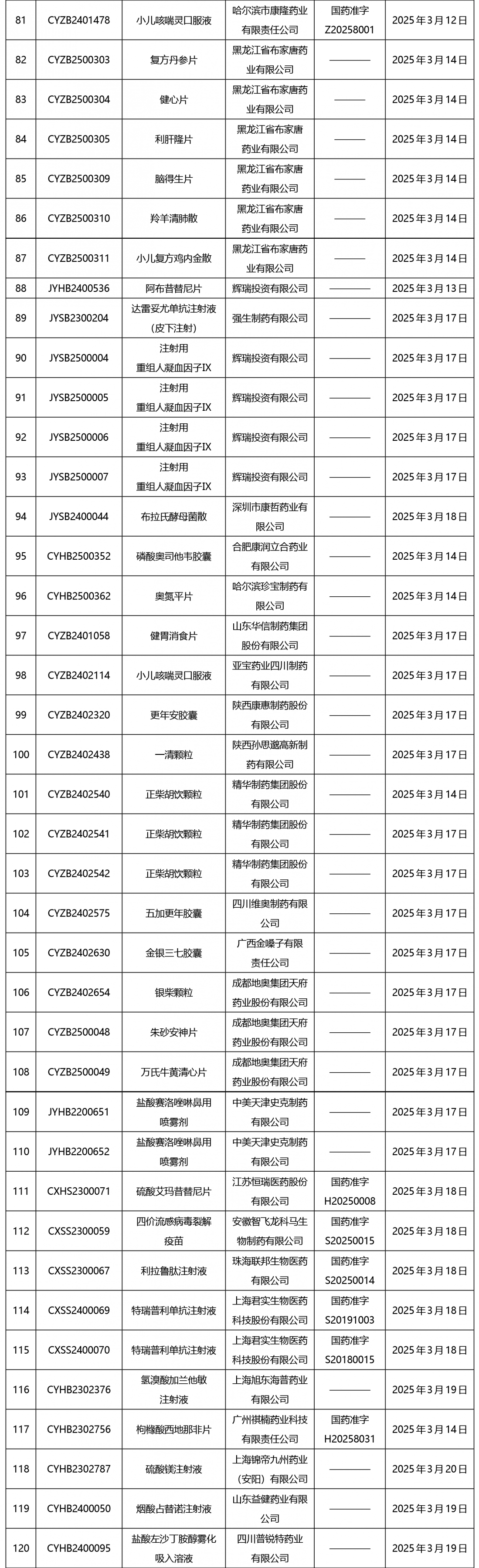
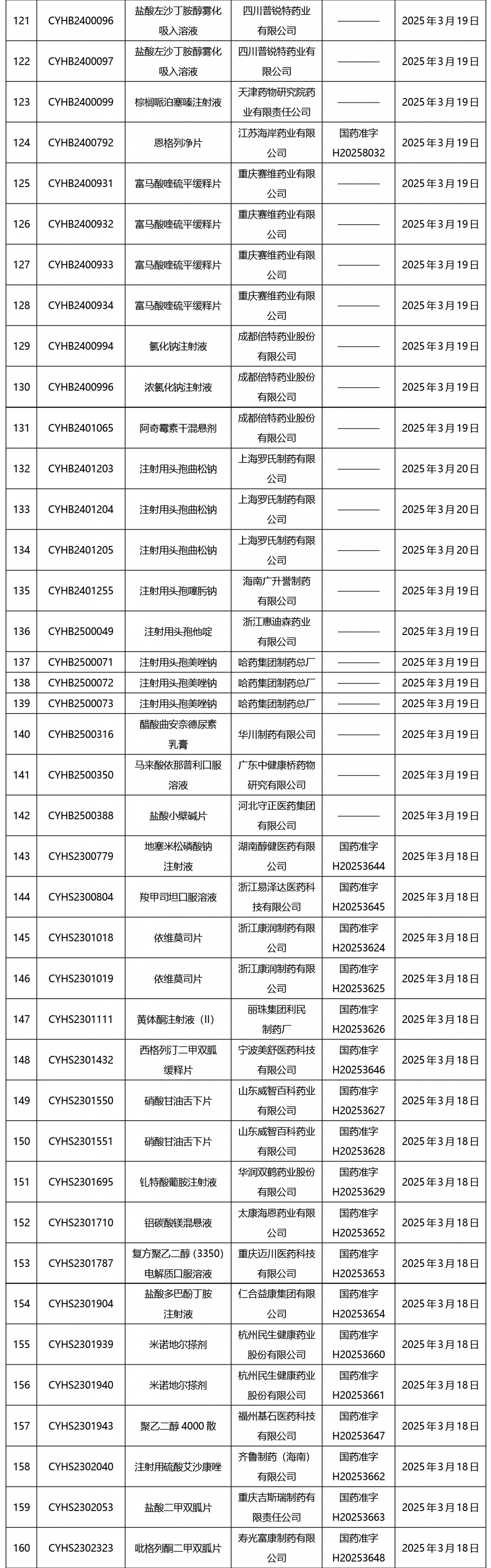

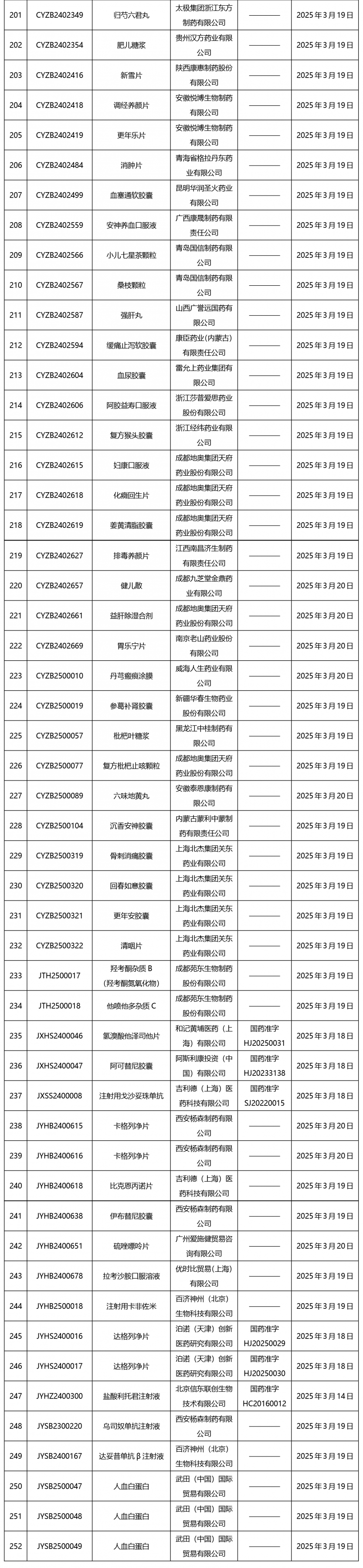
02
國家藥監局綜合司公開征求《藥品生產質量管理規范(2010年修訂)》無菌藥品附錄(征求意見稿)意見
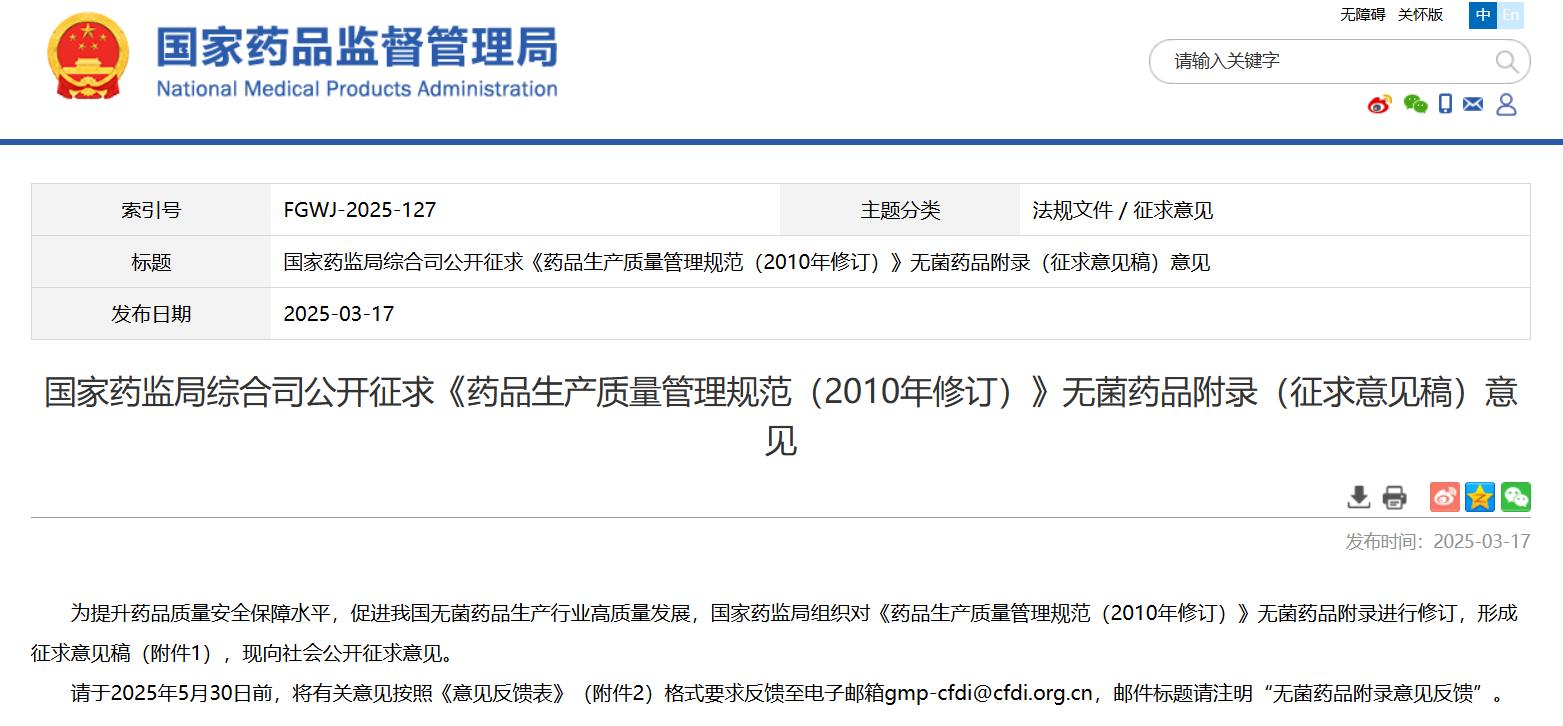
掃描圖中二維碼
查看詳細信息

03
國家藥監局關于47批次不符合規定化妝品的通告(2025年第10號)

掃描圖中二維碼
查看詳細信息

01
關于公開征求《化學仿制藥參比制劑目錄(第九十二批)》(征求意見稿)意見的通知

掃描圖中二維碼
查看詳細信息

-END-


轉載聲明:未經本網或本網權利人授權,不得轉載、摘編或利用其他方式使用上述作品。已經本網或本網權利人授權使用作品的,應在授權范圍內使用,并注明“來源:新領先醫藥科技”。

 Hotline服務熱線:010-61006450
Hotline服務熱線:010-61006450
 簡體中文
簡體中文

 010-61006450
010-61006450 聯系地址:
聯系地址: 技術市場部:
技術市場部: 北京新領先
北京新領先 新領先藥訊
新領先藥訊 010-61006450
010-61006450
